各種活動
小児医薬品開発ネットワーク支援事業
(厚生労働省医政局 医療施設運営費等補助金及び中毒情報基盤整備事業費補助金)
製造販売承認取得品目一覧を追加いたしました(2025年8月)
目的と概要
本事業は、先行して実施された日本医療研究開発機構(AMED)研究事業(平成29年度~令和元年度)の体制を強化し、令和2年度より開始されました。日本小児科学会(以下、学会)が、小児科に関連する専門分科会、小児治験ネットワークと連携し、小児医薬品開発に取り組む製薬企業・治験国内管理人等に対して、開発の企画段階から治験実施、承認申請、及びその後の対応に至るまでの全てのプロセスにおいて、オールジャパン体制で助言・協力・支援します。「医薬品開発は、製薬企業・医療現場・学会が協同して実施する」という意識の浸透、世界同時開発への参画推進やドラッグ・ラグの解消、また小児医薬品開発に関わる人材の育成も目指します。
本事業では、小児医薬品開発のために以下のような活動をしています。
◎規制科学及び医学的見地のみならず、医療現場及び患者・保護者の視点も含めた助言
⇒小児医薬品開発支援チーム(以下、ワーキンググループ)を、相談内容(疾患領域)ごとに迅速に組織します。ワーキンググループには、対象疾患領域の専門医、小児医薬品開発に精通した規制科学・開発薬事専門家、臨床薬理専門家、小児治験の経験が豊富な臨床研究コーディネーターも参加し、多角的な視点から小児医薬品開発に関する助言を受けることができます。
◎小児治験実施のプラットフォームである小児治験ネットワークとの連携による円滑な小児治験の実施
⇒小児治験ネットワークを通じて、フィージビリティ調査、治験実施、中央治験審査委員会での一括審査等を行うことができます。
◎小児医療情報収集システムの活用
⇒小児病院・クリニックの総症例数100万人を超える電子カルテ情報を活用した症例調査等を行うことができます。
事業内容
製薬企業(治験国内管理人等)による小児医薬品開発のご相談や開発支援依頼に対して、学会が中心となりワーキンググループを組織し検討会議を開催します。対象疾患が複数の専門領域にまたがる場合は、複数の分科会による合同ワーキンググループの開催も可能です。小児医薬品開発の専門家より多角的な視点の助言を得られるのみならず、小児治験ネットワークや小児医療情報収集システムも活用することにより、小児治験のための情報収集や実施を迅速かつ効率的に行うことが可能です。
支援内容の例:
- 治験国内管理人・海外企業に対する国内開発の可能性・治験実施体制についての助言
- 開発企画段階での実施可能性やプロトコル骨子案についての助言(開発のgo, no goを決めるためのご相談も可能です)
- 国際共同治験やグローバル開発チームとの連携についての助言(英語対応可能)(例:日本の臨床現場の具体的状況、ニーズや計画の改善点の提案など)
- 医学専門家候補の紹介、対象疾患に関する臨床的知見の提供
- 治験実施計画書、試験デザインに関する助言
- 小児治験ネットワークを通じた実施可能性調査、治験実施施設選定の調査協力、候補施設の提案、中央治験審査委員会事務局の紹介(一括審査は有料)
- 小児医療情報収集システムを活用した、医療機関の該当症例数や、検査値等の診療情報の調査
- 症例登録推進のための助言(遅延の解決策の検討等)、症例検索の協力(学会や小児治験ネットワークを通じた症例調査等)
- PMDAとの対面助言への協力、規制当局からの要望・指摘への対応について協力
- 治験実施中の各種問題に対する具体的助言
- 治験実施体制や安全管理策についての助言
- 承認申請後の規制当局からの照会事項に対する対応・回答についての助言
- 適正使用マニュアル等、医薬品の適正使用に関する助言
本事業へのご相談への対応・助言は、すべて無償で実施いたします。(医学専門家等のご紹介は可能ですが、個別契約は別途ご対応ください)
ワーキンググループを複数回開催することも可能です。
複数の相談例:
- 同じ適応について、国内開発チームとの相談の後、再度グローバルチームも交えた相談を実施
- 実施中の症例集積の遅延の解決についての助言、さらに規制当局からの指示による適正使用マニュアル作成についての助言
- ワーキンググループにて相談の後に、臨床研究コーディネーターに治験実施に関する実務的な相談を実施
- 実施可能性についての助言の後に、治験実施計画案が固まり次第、試験デザイン、治験実施施設選定等について助言
上記の支援内容例に無いご相談事項であっても、ご要望に応じて可能な限り対応・支援します。お気軽に専用メールアドレス(jps-yakuji@jpeds.or.jp ※迷惑メール防止のため、「@」を全角文字にしています。半角文字にして送信してください)までお問い合わせください。
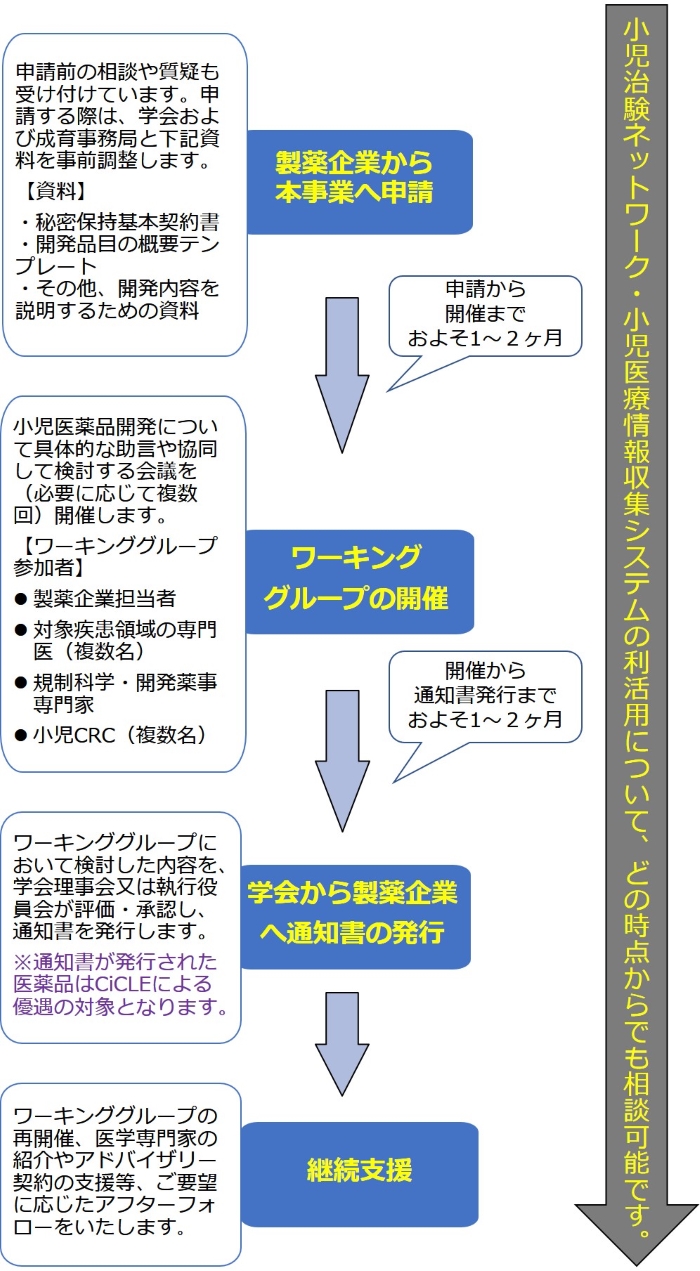
申請と支援の流れ
- 本事業への申請を検討する段階でのお問い合わせなど、事前相談も可能です。
- 本事業への申請は随時受け付けており、締め切りなどは特に定めません。
- 申請からワーキンググループの開催(Webもしくは対面)まで、およそ1~2か月を要しますが、お急ぎの場合はお知らせください。可能な限り対応いたします。
- 一回のワーキンググループ開催時間は、約2時間になります。事前に日時調整を行います。
- ワーキンググループにおいては、開発の概要や支援依頼内容について製薬企業(治験国内管理人等も可)担当者よりご説明いただいた後、質疑及び要望に応じた具体的な助言を含め、小児医薬品開発についてインタラクティブに検討いたします。グローバルの開発メンバーの同席も可能です。
- ワーキンググループの検討結果及び評価結果(分類:「優先」、「通常」もしくは「その他」)が記載された通知書を学会長名で発出します。(評価が「通常」もしくは「その他」とされた品目についても、「優先」とされた品目の開発支援に支障がない限り、「優先」とされた品目と同様の支援を行います)
- 通知書が発出された品目は学会の「開発支援リスト」に掲載され、AMEDの医療研究開発革新基盤創成事業(CiCLE)における採択の審査においても小児を対象とした開発として高く評価され、AMEDに対する成果利用料の支払いなし(通常では売り上げの3%+α)となる優遇制度があります。
- 本事業への申請窓口は日本小児科学会事務局となりますが、国立成育医療研究センターに設置された支援事務局と連携の上で、本事業を円滑に推進します。
成果と企業意見
本事業に対する企業意見(2025年4月現在)
本事業利活用者の事例紹介
事例紹介①
事例紹介②
小児領域における新薬開発促進のための医薬品選定等に関する研究(AMED研究事業)成果概要一覧
手続きについて
1.秘密保持契約について
本事業にはじめて申請される企業におかれましては、企業、学会及び国立成育医療研究センター(本事業の事務局)との3者間の秘密保持に係る契約を締結していただきます。
・秘密保持基本契約様式【契約様式1(第5版)】
・秘密保持基本契約書覚書【契約様式2(第5版)】
※基本契約様式からの追加・修正が必要な場合には、該当箇所が分かるように原則として覚書での対応をお願いいたします。
※締結前(捺印前)に相互に内容を確認するため、基本契約書及び覚書のドラフトを専用メールアドレス(jps-yakuji@jpeds.or.jp ※迷惑メール防止のため、「@」を全角文字にしています。半角文字にして送信してください)まで送付をお願いいたします。
2.提出書類
①開発品目の概要テンプレート(第1版)
②必要に応じて、開発の根拠を説明できる資料を補足してご提出ください。
資料の例(相談に必要と考えられる範囲の書類で結構です、準備が困難であれば、ご相談ください):
- 治験薬に関する概要
- 治験実施計画の概要(治験実施計画書の添付も可能)
- 国際開発の場合、欧米での小児医薬品開発計画書(Paediatric Investigation Plans [PIP]、Pediatric Study Plans [PSP])もしくは計画が分かる概要
- 他適応で承認済みの医薬品であれば添付文書
- 開発計画・概要や相談内容を説明するプレゼン資料(ワーキンググループ開催時に、概要、支援依頼内容についてプレゼンいただきますので、ワーキンググループとのウエブ面談開催までにはご用意ください)
3.提出方法
メールまたは郵便のいずれかでお願いいたします。
●メールによるご提出
PDF形式で、パスワードを設定してください。パスワードは別メールにてお送りください。
専用メールアドレス: jps-yakuji@jpeds.or.jp (※迷惑メール防止のため、「@」を全角文字にしています。半角文字にして送信してください。)
●郵便によるご提出
申請書類をPDF化したファイルをCD-ROMに記録し同封ください。
郵送宛先:〒112-0004 東京都文京区後楽1-1-5 水道橋外堀通ビル4F
公益社団法人日本小児科学会 薬事委員会宛て
※簡易書留、レターパックプラスなど追跡可能な方法で郵送してください。
FAQ
小児医薬品開発ネットワーク支援事業Q&A(2021年9月版)
お問い合わせ
jps-yakuji@jpeds.or.jp
(※迷惑メール防止のため、「@」を全角文字にしています。半角文字にして送信してください。)
参考リンク(AMED研究事業)
平成29年度(2017年度)~令和元年度(2019年度)実施










