各種活動
5~17歳の小児への新型コロナワクチン接種に対する考え方
2022年9月19日(改訂)
2022年8月現在、国内における新型コロナウイルス感染症(以下、COVID-19)の急増に伴い、小児の患者数が増加し、それに応じて重症化する小児患者も増加しています。「新型コロナワクチン~子どもならびに子どもに接する成人への接種に対する考え方~(最終改訂2021年11月)」、「5~11歳小児への新型コロナワクチン接種に対する考え方(最終改訂2022年3月)」を発出した当初から現在にかけて、新型コロナワクチンに関する有効性と安全性に関する情報が多く蓄積されてきました。特に、小児におけるCOVID-19の重症化予防に寄与することが確認されたことをふまえ、メリット(発症予防や重症化予防等)がデメリット(副反応等)を更に大きく上回ると判断し、健康な小児へのワクチン接種は「意義がある」という表現から、「推奨します」という表現に変更する方針としました。以下に理由と考え方を示します。
日本小児科学会は、5~17歳のすべての小児に新型コロナワクチン接種を推奨します。
-
小児患者数の急増に伴い、以前は少数であった重症例と死亡例が増加しています。
-
成人と比較して小児の呼吸不全例は比較的まれですが、オミクロン株流行以降は小児に特有の疾患であるクループ症候群、熱性けいれんが増加し、脳症、心筋炎などの重症例も報告されています。
-
当初はオミクロン株の出現によって新型コロナワクチンの発症予防効果は減弱することが懸念され、重症化予防に関する情報も少ない状況でした。その後は世界各国からの大規模な研究成果が蓄積され、オミクロン株を含めて重症化予防効果が40~80%程度認められることが確認されました。
-
当初は新型コロナワクチンの安全性に関する国内のデータが乏しく、海外のデータに限定されていました。現在では国内の安全性データが集積され、12~17歳における副反応の発生率は、若年成人と同等であり、5~11歳における副反応はより軽い傾向が確認されています。心筋炎・心膜炎の発生報告が稀にあるため注意は必要ですが、発症のリスク因子(10~20歳代の男性)、接種後の症状、発症時期などが明確となり、厚生労働省からの情報提供が充実しています。なお、接種後数日以内に胸痛、息切れ(呼吸困難)、動悸、むくみなどの心筋炎・心膜炎を疑う症状が現れた場合は、すぐに医療機関を受診し、新型コロナワクチンを受けたことを伝えるよう指導してください。新型コロナワクチンを受けた日には激しい運動等は控えるなど、接種後の注意点を子どもたちがよく理解できる様にしてください。
新型コロナワクチン接種の考え方
-
小児をCOVID-19から守るためには、周囲の成人(養育者や小児に関わる業務従事者等)への新型コロナワクチン接種が重要です。周囲の成人が適切な回数(3回目または4回目)の新型コロナワクチン接種を受けることを推奨します。
-
COVID-19重症化リスクが高い基礎疾患のある小児に対しては、重症化予防効果の観点から、年齢にかかわらず新型コロナワクチン接種を推奨します。基礎疾患を有する小児への新型コロナワクチン接種については、本人の健康状況をよく把握している主治医と養育者との間で、接種後の体調管理等を事前に相談することが望ましいと考えます。詳細については「新型コロナワクチン接種に関する、小児の基礎疾患の考え方および接種にあたり考慮すべき小児の基礎疾患等」を併せてご参照ください。
-
日本小児科学会は5~17歳の健康な小児への新型コロナワクチン接種を推奨します。健康な小児への新型コロナワクチン接種には、メリット(発症予防・重症化予防等)とデメリット(副反応等)を本人と養育者が十分理解することが重要です。その際に参考となる小児における新型コロナワクチンの安全性・有効性に関する情報が収集されつつあり、小児においてもその効果と安全性が確認されています。実際に接種する際には接種前・中・後にきめ細やかな対応が必要で、同調圧力が加わらないような配慮が必要です。
-
2回目の接種から5か月以上経過した12~17歳の小児に対しては、早期の追加接種(3回目)を推奨します。
-
新型コロナワクチン接種担当者は接種にあたっては、接種対象年齢による製剤の取り扱いに注意することが必要です。12歳以上用、5~11歳用の新型コロナワクチンでは、製剤・希釈方法・接種量・接種回数・保管方法が異なります。接種部位についても筋肉量の少ない一部の小児では大腿四頭筋への接種が推奨されます。また、集団接種を実施する場合においても、個別接種に準じて、接種前の問診と診察を丁寧に行い、定期接種ワクチンと同様の方法で実施するとともに、母子健康手帳への接種記録を行うことが望ましいと考えます。
-
「新型コロナワクチン~子どもならびに子どもに接する成人への接種に対する考え方~(2021年11月2日改訂)」
-
「5~11歳小児への新型コロナワクチン接種に対する考え方(2022年3月28日一部修正)」
-
「12~17歳の小児に対する新型コロナワクチン追加接種について(2022年3月25日)」
1. 感染状況に関する知見
-
小児のCOVID-19症例の95%以上は軽症ですが、クループ症候群、肺炎、けいれん、嘔吐・脱水などの中等症や、心不全をきたしうる小児多系統炎症性症候群、脳症および心筋炎が報告されています1)~8)。国内における10歳未満、10歳代のCOVID-19による死亡報告数はオミクロン株流行前の2021年末においてはそれぞれ0例、3例でしたが、オミクロン株流行以降のわずか7か月で、それぞれ8例、6例の死亡が報告されており、20歳未満における累積死亡者数は17例まで増加しています(2022年7月26日現在)9)。また、COVID-19流行初期は小児感染者が全体に占める割合は低い状況でしたが、2022年1月以降は10歳未満の小児が占める割合は10~20%程度、10歳代を含めると30%程度となっています9)。
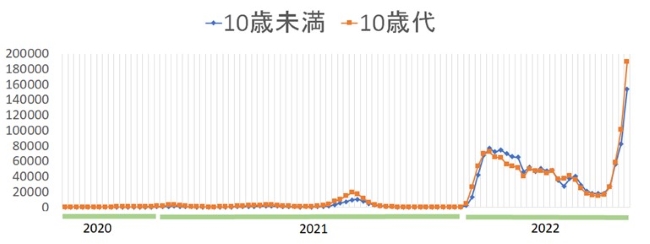 小児新規陽性者数の推移 厚生労働省の公表資料を基に作図https://covid19.mhlw.go.jp
小児新規陽性者数の推移 厚生労働省の公表資料を基に作図https://covid19.mhlw.go.jp
-
国内の小児における症状を流行株の違いにより分けた場合に、オミクロン株流行期における患者は発熱の頻度が高く、熱性けいれん、咽頭痛、嘔吐の報告数が多いことが確認されています10)。
-
2歳未満(0~1歳)と基礎疾患のある小児患者において重症化リスクが増大することが報告されています1) 11)。
-
長期化する流行による行動制限が小児に与える直接的および間接的な影響は大きくなっています。さらに、オミクロン株流行に伴う小児患者数の増加に伴い、保育施設12)、学級、学校閉鎖13)の数が増加しています。
-
小児への感染は周囲の成人からの伝播が多くを占めていましたが、オミクロン株流行以降、小児同士で感染する機会が増加しています。更にオミクロン株流行前においては1割程度であった感染源不明の小児例は、オミクロン株流行以降2割以上まで増加しており、特に2022年6月以降の直近2か月においては、感染源不明の小児症例が約3割を占めるようになっています14)。
2. ワクチンに関する知見
-
製剤について:国内で5~11歳への接種が承認されているワクチンは、現時点ではファイザー社製のみです。同ワクチンは12歳以上の人に接種するワクチンと比べ含有されるmRNA量が1/3の製剤で、1回接種量も0.2 mLと異なっており、使用に際し注意が必要です15)。
-
有効性について:海外では、5~11歳の小児に対する同ワクチンの発症予防効果は当初90%以上と報告されていました16)。一方、流行株がオミクロン株に変わってからの感染予防効果は31%、救急外来受診予防効果は51%と低下していますが17)18)、入院予防効果は68%と報告されています19)。その後、オミクロン株流行期における5~11歳の小児へのワクチン有効性については、世界各国から報告が相次ぎ、既報と同様の発症予防効果と重症化予防効果が確認されています21)~23)。また、ワクチン接種によって、COVID-19の重症合併症の一つである小児多系統炎症性症候群の発症を約90%防げることもわかっています20)。その一方で、5~11歳用のワクチンは12歳以上用のワクチンよりは効果が落ちること、接種後の時間経過とともに減衰することが確認されています21)~23)。
-
安全性について:米国では、2021年11月3日~12月19日までに5~11歳の小児に約870万回のファイザー社製ワクチンが接種され、42,504人が自発的な健康状況調査(v-safe)に登録されました。2回接種後、局所反応が57.5%、全身反応が40.9%に認められ、発熱は1回目接種後7.9%、2回目接種後13.4%に認められました24)。上記と同期間に、米国の予防接種安全性監視システム(VAERS)には、4,249件の副反応疑い報告がありました。このうち97.6%(4,149件)が非重篤でした。重篤として報告された100件(2.4%)の中で最も多かったのが発熱(29件)でした24)。接種後の心筋炎は、2回接種後100万接種当たり男児2.7件、女児0.8件と、いずれも12歳以上と比べて少なくなっています(2022年4月21日までのデータ)25)。国内では、2022年6月12日までに5~11歳の小児に推定2,464,581回(1回目・2回目の総数)のファイザー社製ワクチンが接種され、医療機関から副反応疑いとして報告されたのが、1回目は0.0047%(62件)、2回目は0.0033%(38件)と12歳以上よりも低い頻度でした。製造販売企業から報告された心筋炎疑い例は男女合わせて6件で、2回接種後100万回接種当たり2.6件と、米国男児の報告と変わりませんでした26)。副反応の詳細を調査した岡山県の報告でも、小児は成人より接種後早期の副反応が軽い傾向にありました27)。
-
製剤について:国内で12~17歳を対象とする1・2回目の接種への承認がされているワクチンは、現時点ではファイザー社製およびモデルナ社製の2製剤です。それぞれ成人に対するワクチンと同じ製剤です。
-
有効性について:現在、国内で流行しているオミクロン株へのワクチンの効果については、海外において12~15歳を対象として行われたファイザー社製ワクチンの感染予防効果に関する研究が行われ、ワクチン2回接種から14~149日経過後で59%でした17)。また、12~17歳を対象として行われた研究では、新型コロナワクチン2回接種から14~149日経過後の入院予防効果はデルタ株とオミクロン株が混在する時期において、12~15歳で92%、16~17歳で94%でした18)。さらに、致命的な症状(集中治療を要する症状の出現)や小児多系統炎症性症候群に対する予防効果も報告されています19)20)。
-
安全性について:新型コロナワクチン接種後に出現する症状としては、軽微なものでは、発熱、頭痛、局所反応などが多く、重篤なものとしては、アナフィラキシーや血栓症、心筋炎・心膜炎などが挙げられます。国内では2022年6月12日までに、12~17歳に対する1・2回目までの新型コロナワクチン接種回数はファイザー社製およびモデルナ社製の合計9,687,771回で、医療機関から合計936件(うち重篤306件)の副反応が疑われる事例が報告されました28)。報告頻度は0.0097%であり、18~24歳の報告頻度の0.0215%と比較して少ない傾向が見られました。12~17歳で生じる重篤な副反応のうち、特筆すべきものとしては、心筋炎・心膜炎が挙げられます。国内で2022年6月10日時点までに製造販売企業から報告された12~14歳の新型コロナワクチン接種後心筋炎疑い報告の頻度は、いずれも100万回接種あたりで、ファイザー社製の1回目男子5.6件、1回目女子2.0件、2回目男子41.6件、2回目女子4.0件、モデルナ社製の1回目男子18.5件、1回目女子0.0件、2回目男子103.5件、2回目女子0.0件でした26)。米国の集計データでも同様の報告がなされていますが、12~29歳の新型コロナワクチン関連心筋炎患者398人のうちその後のフォロ―で66.6%が完全に回復したことが確認され、15.1%は回復(最終確認待ち)、15.3%は軽快傾向、2.0%は不明、1.0%は軽快していないことが確認されています29)。なお、米国で行われたデータベースを用いた研究ではCOVID-19感染者における心筋炎発症のリスクは0.146%であったのに対して非感染者におけるリスクは0.009%でした30)。現時点では新型コロナワクチンの長期的な安全性に関わる情報は少ないので、今後も注意が必要です31)。なお、万が一、起こりうる心筋炎・心膜炎に対して、接種後2週間の激しい運動の制限を行っている国もあります(シンガポール https://www.vaccine.gov.sg/health-advisory/)。
-
対象について:2022年3月以降、日本でも12~17歳の小児に対する新型コロナワクチンの追加接種が認められています。また2022年9月6日からは、5~11歳の小児に対しても追加接種が認められています。18歳未満への追加接種が認められているのはファイザー社製ワクチンのみです。
-
有効性について:国内では、現在オミクロン株の流行が継続しています。デルタ株に比してオミクロン株では、発症予防効果、重症化予防効果の減衰が早く、追加接種により効果が回復することが報告されています18)。オミクロン株流行期における12~15歳の小児に対する追加ワクチン(3回目)の発症予防効果は接種後2~6.5週時点で71.1%と報告されています32)。
-
安全性について:12~17歳の小児への追加接種が実施されている米国から、新型コロナワクチン接種後の初回免疫後(2回目)と追加免疫後(3回目)の局所反応はそれぞれ77.8%と82.0%、全身反応はそれぞれ77.2%と77.8%と大きな差はなく、追加接種後に入院を要した患者は3,418人中1名(片頭痛のため)と稀であったと報告されています33)。国内の副反応疑い報告制度に基づく報告割合は心筋炎も含めて、ファイザー社製ワクチンの2回目より3回目接種において、12~14歳で100万接種あたり男子10.1件、女子0.0件と少ないことが確認されています26)。
-
18歳以上の成人を対象としたtest negative designを用いた検討では、2021年6~7月(デルタ株49%)における発症予防効果は92%、8~9月(デルタ株89%)において79%でした。入院予防効果は97%と報告されています34)。
-
デルタ株流行期(2021年8月から9月)とオミクロン株流行期(2022年1月から3月)までに複数医療機関の発熱外来等を受診した成人(20歳以上)を対象とした調査では、新型コロナワクチン接種による発症予防効果はデルタ株流行期で88%(2回接種後14日~3か月)、87%(2回接種後3~6か月)、オミクロン株流行期で56%(2回接種後14日~3か月)、52%(2回接種後3~6か月)、49%(2回接種後6か月以上)、74%(3回接種後14日以上)が確認されました35)。
-
宮城県において2021年8~9月のデルタ株流行期において18歳以上の接触者を対象とした検討では、感染予防効果は50~80%と推計されています36)。
-
東京都の全年齢を対象とした検討では、2022年1月のオミクロン株流行期における有効性はデルタ株流行期と比べ62.1%(95% CI:48~66%)に低下しています37)。
-
静岡県における公開データ(静岡県健康福祉部新型コロナ対策企画課・推進課)によると、各年代あたりの接種割合と感染者の発生数(人口10万人当たりの週間感染者数)は逆相関し、被接種者が少ない小児における発症が多いことが確認されています。また、オミクロン株流行期(2022年5~7月)における5~11歳を対象とした検討でも、2回接種者は未接種者と比較して感染者の割合が30~60%程度であることが確認されています38)。
上記のことから、国内においても海外からの報告と同様の有効性が期待されます。
日本の小児における新型コロナワクチンの安全性、有効性のデータを引き続き収集し、この考え方を随時検証し、更新していきます。
本件に関する問い合わせは、情報管理の観点から、FAXのみに限らせていただきますことをご理解いただけますようお願い申し上げます(対応には日数を要すること、個別のお問い合わせには対応できない場合もありますことを予めご了承ください)。
<お問合せ先>
公益社団法人日本小児科学会事務局
〒112-0004
東京都文京区後楽1-1-5水道橋外堀通ビル4階
FAX:03-3816-6036










